6.6 Eigenschaften und Verwendung der Carbonsäuren

Eigenschaften
- abhängig von der Carboxygruppe (–COOH)
- das Sauerstoffatom der Carbonylgruppe (C=O) weist einen relativ starken elektronenziehenden Effekt auf, sodass die Bindung zwischen dem H-Atom und dem O-Atom der Hydroxygruppe stark polarisiert wird – wodurch die Freisetzung des Wasserstoffs als H+-Ion möglich wird
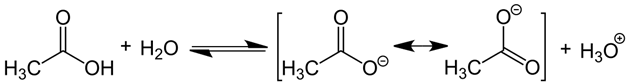
- saurer Charakter: in der Reaktion mit Wasser erfolgt ein Protonenübergang (Protolyse der Säure) unter Bildung eines mesomeriestabilisierten Carboxylat-Anions (stabile Forme der Säure, delokalisierte Elektronen) und Oxoniumionen
- Acidität (= Maß für die Fähigkeit einer chemischen Verbindung Protonen abzugeben) steigt, wenn am α-C-Atom ein Substituent mit elektronenziehendem Effekt vorliegt (Carboxygruppe erhält eine positivere Partialladung, welche die negative Ladung des Anions stabilisiert werden) (z.B. Vergleich Acetat und Trichloracetat)
- kurzkettige Carbonsäuren sind farblose, stark riechende Flüssigkeiten
- polarer Charakter der Carboxygruppe führt zu relativ hohen Siedetemperaturen (Ausbildung von WBB)
- zunehmende Kettenlänge des Alkylrestes der Carbonsäuren und deren Salze führt zur Zunahme des lipophilen Charakters und zur Abnahme des hydrophilen Charakters
z.B. häufigsten Fettsäuren mit 16 oder 18 C-Atomen, ihre Triglyceridester sind Fette, die Natrium- und Kaliumsalze der Fettsäuren zeigen Tensideigenschaften und werden als Seifen verwendet
Verwendung
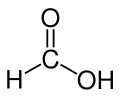
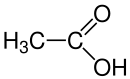
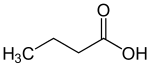
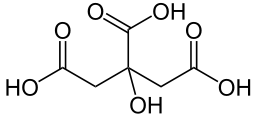
Auswahl einiger wichtiger Carbonsäuren:
|