2.1.1 Die Elementarteilchen
Die Elektronen
Bereits um 1700 konnte man in Glasröhren, in denen man einen Unterdruck erzeugt hatte, durch elektrische Entladungen zwischen Kathode und Anode Leuchterscheinungen erzeugen. Man erkannte bald, dass die Leuchtfarben von der Art des verwendeten Gases abhingen. Diese so erzeugten Leuchterscheinungen ließen sich durch ein Magnetfeld ablenken, also mussten sie von einem Strahl negativ geladener Teilchen verursacht sein, die vom negativen Pol, der Kathode, ausgingen. 1876 wurde die Bezeichnung „Kathodenstrahl“ vorgeschlagen. Die Kathodenstrahlröhre wurde 1897 von Ferdinand Braun entwickelt, weshalb sie auch Braunsche Röhre genannt wird. Anfangs war nicht bekannt, dass die von der Kathode ausgehende Strahlung aus Elektronen besteht, daher verwendete man dafür die Bezeichnung Kathodenstrahlen.
Die Abbildung zeigt das Schema eines Kathodenstrahlrohres.
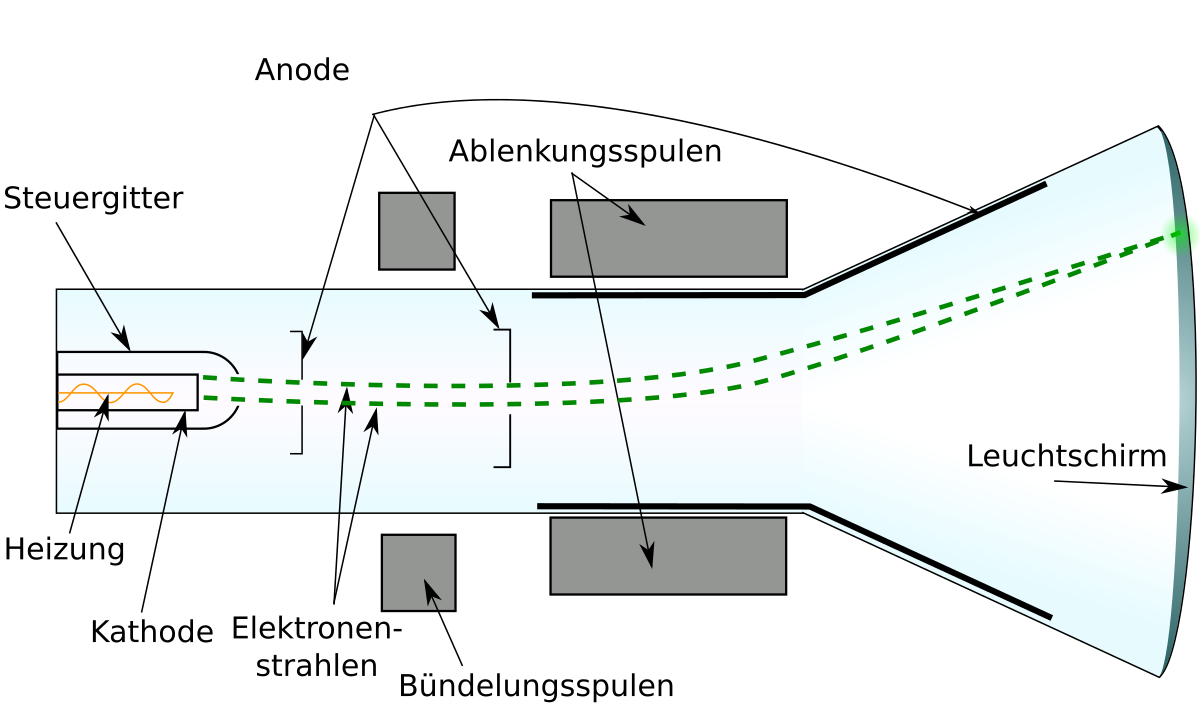
By FischX, Interiot, Raster:Theresa Knott – This file was derived from: Cathode ray tube diagram-en.svg, CC BY-SA 3.0, Link
Im selben Jahr entdeckte man, dass sich ein bewegliches Rädchen zu dehen begann, wenn man die Kathodenstrahlen darauf richtete.
1896 bewies Joseph J. Thomson (1856 – 1940), dass es sich bei den Kathodenstrahlen, die durch elektrische und magnetische Felder ablenkbar waren, um elektrische Teilchen handelte, deren Masse er als etwa ein Tausendstel der des leichtesten Atoms (des Wasserstoffatoms) bestimmte. Der genaue Wert liegt bei 1 : 1837.
Da die Teilchen der Kathodenstrahlen in ihren Eigenschaften unabhängig vom verwendeten Kathodenmaterial und der Gasfüllung waren, blieb nur die Deutung, dass sie Bestandteil aller Atome sein mussten. Bereits 1891 hatte man für diese Teilchen den Begriff „Elektronen“ eingeführt.
Eigenschaften der Elektronen:
| Symbol | Ladung (e)* | Masse (u)** | Masse (g) |
| e– | – 1 e | 0,00055 | 9,109 . 10-28 |
| e* Elementarladung (1 e = 1,602 . 10-19 Coulomb) | |||
| u** Atomare Masseneinheit | |||
Die Protonen
Im Zuge der Untersuchung der Kathodenstrahlen entdeckte E. Goldstein 1886 das Proton. Er beobachtete bei einer Kathode, in die ein Loch gebohrt war, eine Strahlung. Ihre Richtung war der der Kathodenstrahlen entgegengesetzt.
Die verwendete Apparatur heißt Kanalstrahlrohr. Es ist mit Wasserstoff gefüllt, der nur unter geringem Druck steht. Die Elektronen treffen auf ihrem Weg von der Kathode zur Anode mit so hoher Geschwindigkeit auf die Wasserstoffteilchen, dass die Wasserstoff-Moleküle (H2) in Atome gespalten werden, und diesen ihr einziges Elektron entrissen wird (Stoßionisierung im elektrischen Feld). Vom Wasserstoffatom bleibt nur der Kern, also das Proton übrig, das in Richtung Kathode beschleunigt wird und durch das dort vorhandene Loch tritt.
Er bezeichnete die neu entdeckten Strahlen als „Kanalstrahlen“. Sie waren nur mit einem sehr starken Magneten ablenkbar. Die Richtung der Ablenkung war der der Kathodenstrahlen entgegengesetzt, also musste auch die Ladung der Elektronen entgegengesetzt sein. Die Masse eines Protons wurde von Ernest Rutherford bestimmt. Sie war 1837mal so groß wie die des Elektrons und entsprach praktisch damit der des Wasserstoffatoms.
Eigenschaften der Protonen:
| Symbol | Ladung (e) | Masse (u) | Masse (g) |
| p+ | + 1 e | 1,0078 | 1,673 . 10-24 |
Die Neutronen
Sie wurden erst relativ spät, nämlich 1932 von dem Mitarbeiter Rutherfords, James Chadwick, entdeckt. Man experimentierte auf der Suche nach den Kernkräften mit leichten Atomkernen wie Beryllium, die man mit Alphateilchen bestrahlte. Aus dem Beryllium mussten Teilchen ausgetreten sein, die selbst in einer Nebelkammer keine Spuren hinterließen. Aus einem Paraffinblock, der in der Nebelkammer angebracht war, beobachtete er die Spur eines Protons. Es waren also unsichtbare Teilchen in das Paraffin eingedrungen und hatten das Proton herausschlagen können.
Eigenschaften der Neutronen:
| Symbol | Ladung (e) | Masse (u) | Masse (g) |
| n | 0 | 1,0087 | 1,675 . 10-24 |
