Übungsaufgaben – Orbitaltheorie und Aufenthaltswahrscheinlichkeit von Elektronen in der Atomhülle
Aufgaben: Orbitaltheorie und Aufenthaltswahrscheinlichkeit von Elektronen in der Atomhülle
Sie benötigen das Periodensystem der Elemente!
- Die Perioden im PSE (= Energiestufen) werden den Hauptniveaus der Orbitaltheorie gleichgesetzt. Je nach Hauptniveau können verschiedene Unterniveaus zugeordnet werden. Benennen Sie die Unterniveaus, ordnen Sie die Anzahl der Orbitale und die maximal mögliche Elektronenanzahl zu.
- Formulieren Sie die Regeln zur Besetzung der Unterniveaus mit Elektronen.
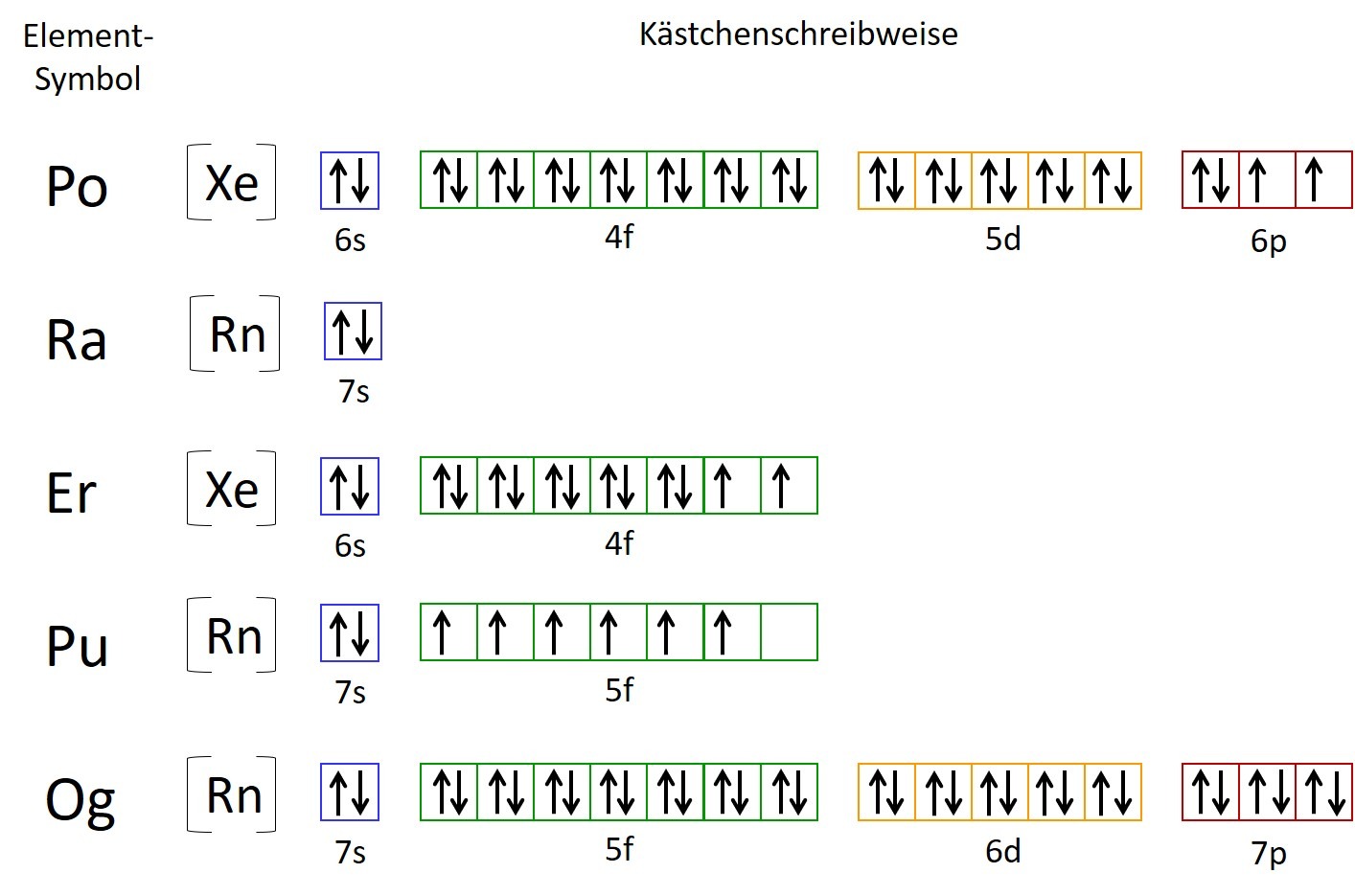
- Die Verteilung der Elektronen eines Elements in der Atomhülle lässt sich im Rahmen der Orbitaltheorie durch zwei Möglichkeiten darstellen – in Kästchenschreibweise oder Elektronenkonfigurationsschreibweise. Notieren Sie beide Schreibweisen für die folgenden Elemente: Po, Ra, Er, Pu, Og
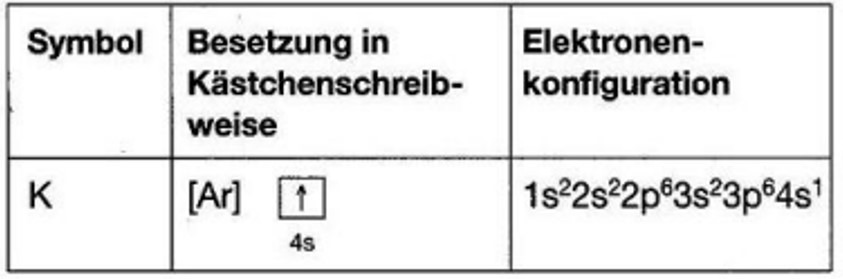
- Geben Sie die Quantenzahlen als Aufenthaltskoordinaten in der Atomhülle für das 2., 9. Und 13. Elektron des Chlor-Atoms an.