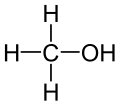
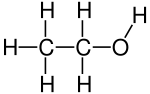
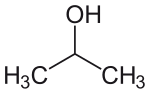
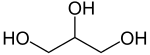
6.3 Eigenschaften und Verwendung der Alkohole

Physikalische Eigenschaften
Aggregatzustand, Geruch und Geschmack:
- niedrigmolekulare Alkohole sind Flüssigkeiten, die einen charakteristischen Geruch und einen brennenden Geschmack besitzen
- höhere Alkohole sind meist feste Verbindungen mit nur schwach ausgeprägtem Geruch
Löslichkeit:
- sind amphiphil, aufgrund des hydrophilen Charakters der Hydroxygruppe und des hydrophoben Charakters der Alkylkette (kurzkettige Alkohole sind gute Lösungsmittel)
- mit zunehmender Länge der Alkylkette – Abnahme des hydrophile Charakters
- mit zunehmender Anzahl der Hydroxygruppen – Zunahme des hydrophilen Charakters
Schmelz- und Siedepunkte:
- besitzen aufgrund intermolekularer Wasserstoffbrückenbindungen relativ hohe Schmelz- und Siedepunkte gegenüber Alkanen mit vergleichbarer molarer Masse (z.B. unpolares Ethan (C2H6) (M = 30) mit Sdp. von −89 °C, Methanol (CH3OH) (M = 32) Sdp. von 65 °C)
- Erhöhung der Siedepunkte mit zunehmender Länge der Alkylkette und zunehmender Anzahl der Hydroxygruppen
- Erniedrigung der Siedepunkte, je verzweigter und kugelförmiger die Moleküloberfläche ist und je mittelständiger die Hydroxygruppen in den Molekülen liegen (Abnahme der van-der-Waals-Wechselwirkungen)
- unverzweigte, langgestreckte, primäre Alkohole besitzen höhere Siedepunkte
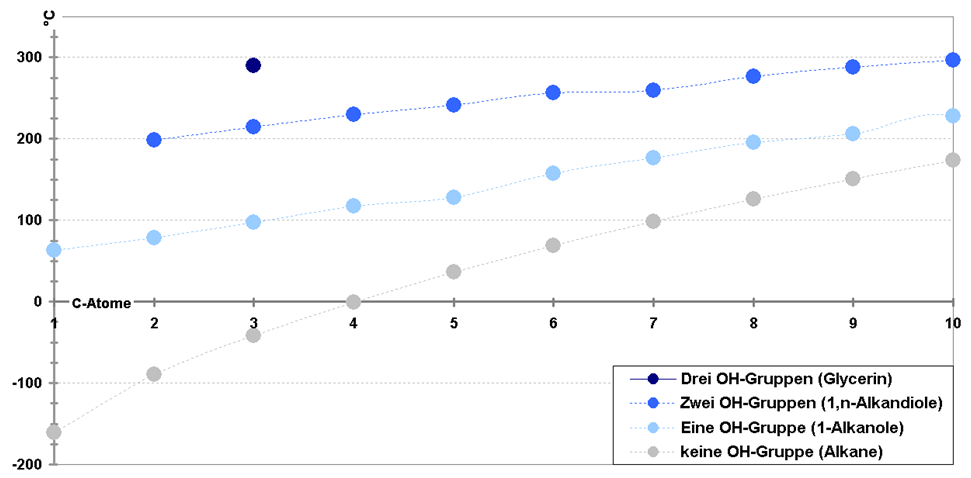
Von Peter Krimbacher – Selbst erstellt (openOffice und Screenshot): Abhängigkeit der Siedepunkte von der Anzahl der OH-Gruppen, CC BY-SA 2.0 de, https://commons.wikimedia.org/w/index.php?curid=9003528
Verwendung
Viele Alkohole sind wichtige Lösungsmittel, die sowohl in der Industrie, als auch im Haushalt eingesetzt werden. Die mengenmäßig wichtigsten sind dabei Methanol, Ethanol, 2-Propanol und n-Butanol. Im Jahr 2011 wurden weltweit etwa 6,4 Mio. Tonnen dieser alkoholischen Lösungsmittel verbraucht.
Übersicht über einige wichtige Alkohole:
|