4.2 Nomenklatur und räumlicher Bau organischer Verbindungen
Die organische Chemie beschäftigt sich mit den Strukturen und Reaktionen organischer Verbindungen. Darunter versteht man die Verbindungen des Kohlenstoffs mit Ausnahme der Chalkogenide wie z. B. Kohlenstoffmonooxid (CO) oder Kohlenstoffdioxid (CO2), der Carbide, der Kohlensäure (H2CO3) und ihrer Salze, sowie der Metallcarbonyle (M[CO]x). Diese werden der Anorganischen Chemie zugeordnet.
Die grundlegenden Verbindungen der organischen Chemie stellen die Kohlenwasserstoffe dar, bei denen neben Kohlenstoff noch Wasserstoff enthalten ist. Darüber hinaus können organische Verbindungen auch andere Atome wie Sauerstoff oder Stickstoff, seltener auch Schwefel, Phosphor oder Halogene enthalten.
Obwohl am Aufbau der organischen Moleküle nur so wenige Atomsorten beteiligt sind, überwiegt die Anzahl der bekannten organischen Verbindungen (heute etwa 15 Millionen) die der anorganischen Verbindungen (etwa 300000) erheblich. Dies liegt vor allem an der Fähigkeit der Kohlenstoffatome auch untereinander Einfach- oder auch Mehrfachbindungen eingehen zu können. Dadurch können kettenartige Moleküle entstehen mit praktisch unbegrenzter Anzahl an Kohlenstoffeinheiten. Durch Verzweigung dieser Ketten oder Ringschlüsse kann eine große Vielfalt unterschiedlicher Strukturen entstehen.
Diese Vielzahl an organischen Verbindungen unterteilt man in bestimmte Stoffklassen, die nach dem Vorliegen bestimmter Atomsorten oder nach funktionellen Gruppen bezeichnet werden. Zu solchen Derivaten der Kohlenwasserstoffe (Alkane, Alkene, Alkine) zählen Alkhole, Aldehyde und Ketone, Carbonsäuren, Ether und Ester. Als Derivate werden in der Chemie abgeleitete Stoff mit ähnlicher Struktur bezeichnet. Sie besitzen an Stelle eines H-Atoms entweder ein anderes Atom oder eine ganze Atomgruppe oder es wurden ein oder mehrere Atome / Atomgruppen entfernt.
| Alkane | Alkene | Alkine |
 |
 |
 |
In der Chemie der Kohlenwasserstoffe werden die strukturgebenden Stoffgruppen Alkane, Alkene und Alkine unterschieden, in Abhängigkeit der enthaltenen Einfach- oder Mehrfachbindungen.
Alkane
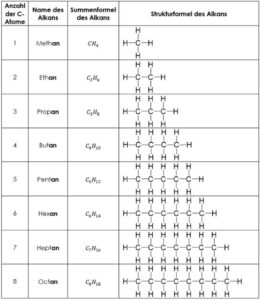
Gesättigte Kohlenwasserstoffe, in denen nur Einfachbindungen von den C-Atomen ausgehen, werden als Alkane bezeichnet. Mit der Endsilbe -an im Stoffnamen wird auf den gesättigten Charakter der Verbindung hingewiesen.
Ausgehend vom einfachsten Alkan, dem Methan, lässt sich formal durch Einschub jeweils einer CH2-Gruppe die homologe Reihe der Alkane aufbauen.
Homologe Reihe:
Eine Reihe zusammengehörender Verbindungen, deren aufeinanderfolgende Glieder sich jeweils um ein Kettenglied unterscheiden, werden als homologe Reihe bezeichnet. Für alle diese Glieder kann eine allgemeine Summenformel angegeben werden.
Allgemeine Summenformel: CnH2n+2
Isomerie
Die Kohlenstoff-Ketten der Alkane können verzweigt oder unverzweigt sein. Für die Summenformel C4H10 lassen sich daher zwei Strukturformeln entwickeln. Dies ist einerseits eine unverzweigte Kohlenstoff-Kette aus vier C-Atomen. Dieses Molekül wird als n-Butan (“Normalbutan”) bezeichnet. Andererseits kann eine Kette von drei C-Atomen gebildet werden, wobei das mittlere mit einem weiteren C-Atom verbunden ist. Diese verzweigte Form wird als Isobutan bezeichnet. n-Butan und Isobutan sind Konstitutionsisomere, sie besitzen dieselbe Summenformel, unterscheiden sich jedoch in ihrer Struktur.
Nomenklatur
Die Nomenklatur nach IUPAC (International Union of Pure and Applied Chemistry) ist eine Systematik zur exakten Benennung von Molekülen mit unterschiedlicher Struktur nach den folgenden Regeln:
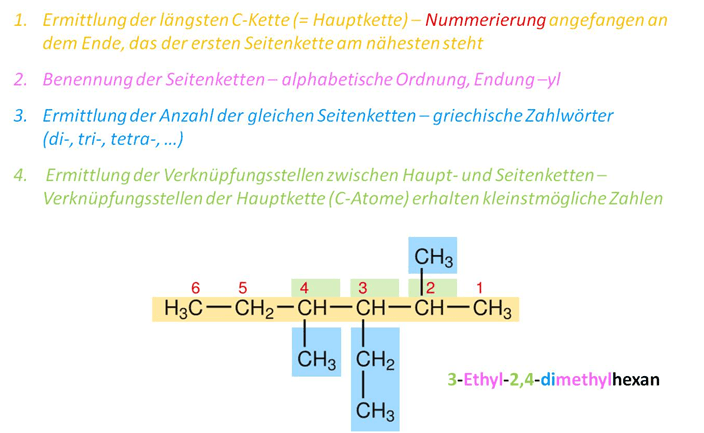
© Belinda Flemming: Nomenklatur nach IUPAC für die Benennung von Kohlenwasserstoffen, CC BY-SA
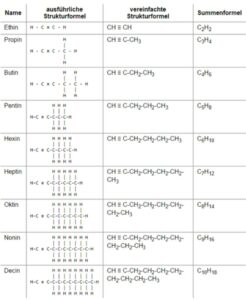
Alkene
Ungesättigte Kohlenwasserstoffe mit C=C-Doppelbindungen werden nach der Genfer Nomenklatur als Alkene bezeichnet. Die Bezeichnung ungesättigt deutet darauf hin, dass jedes der an der Doppelbindung beteiligten Kohlenstoffatomen ein Wasserstoffatom weniger bindet. Im Namen wird dies durch die Endung -en ausgedrückt. Durch Aufnahme von Wasserstoff können die Alkene in die gesättigten Alkane übergehen.
Liegt nur eine Doppelbindung vor, so kann folgende allgemeine Summenformel formuliert werden: CnH2n
Homologe Reihen der Alkene:

Alkine
Diese ungesättigten Verbindungen unterscheiden sich von den Alkanen dadurch, dass sie 4 Wasserstoffatome weniger als die Alkane aufweisen und damit eine Dreifachbindung enthalten. Die Bezeichnung schließt mit der Endsilbe -in. Die Monoalkine, Alkine also mit nur einer Dreifachbindung, bilden demnach eine homologe Reihe mit folgender allgemeiner
Summenformel: CnH2n-2
Homologe Reihe: